Содержание
Электрохимическая защита от коррозии состоит из катодной и дренажной защиты. Катодная защита трубопроводов осуществляется двумя основными методами: применением металлических анодов-протекторов (гальванический протекторный метод) и применением внешних источников постоянного тока, минус которых соединяется с трубой, а плюс – с анодным заземлением (электрический метод).
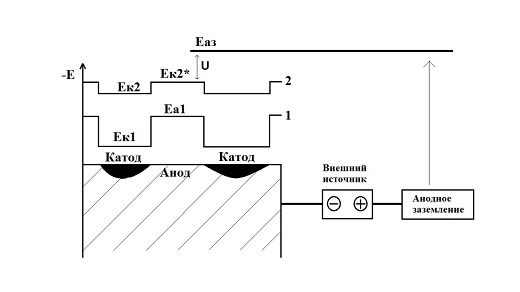
Рис. 1. Принцип работы катодной защиты
Гальваническая протекторная защита от коррозии
Наиболее очевидным способом осуществления электрохимической защиты металлического сооружения, имеющего непосредственный контакт с электролитической средой, является метод гальванической защиты, в основу которого положен тот факт, что различные металлы в электролите имеют различные электродные потенциалы. Таким образом, если образовать гальванопару из двух металлов и поместить их в электролит, то металл с более отрицательным потенциалом станет анодом-протектором и будет разрушаться, защищая металл с менее отрицательным потенциалом. Протекторы, по существу, служат портативными источниками электроэнергии.
В качестве основных материалов для изготовления протекторов используются магний, алюминий и цинк. Из сопоставления свойств магния, алюминия и цинка видно, что из рассматриваемых элементов магний обладает наибольшей электродвижущей силой. В то же время одной из наиболее важных практических характеристик протекторов является коэффициент полезного действия, показывающий долю массы протектора, использованной на получение полезной электрической энергии в цепи. К.П.Д. протекторов, изготовленных из магния и магниевых сплавов, редко превышают 50 % в, в отличие от протекторов на основе Zn и Al с К.П.Д. 90 % и более.


Рис. 2. Примеры магниевых протекторов
Обычно протекторные установки применяются для катодной защиты трубопроводов, не имеющих электрических контактов со смежными протяженными коммуникациями, отдельных участков трубопроводов, а также резервуаров, стальных защитных кожухов (патронов), подземных резервуаров и емкостей, стальных опор и свай, и других сосредоточенных объектов.
В то же время протекторные установки очень чувствительны к ошибкам в их размещении и комплектации. Неправильный выбор или размещение протекторных установок приводит к резкому снижению их эффективности.
Катодная защита от коррозии
Наиболее распространенный метод электрохимической защиты от коррозии подземных металлических сооружений – это катодная защита, осуществляемая путем катодной поляризации защищаемой металлической поверхности. На практике это реализуется путем подключения защищаемого трубопровода к отрицательному полюсу внешнего источника постоянного тока, называемого станцией катодной защиты. Положительный полюс источника соединяют кабелем с внешним дополнительным электродом, сделанным из металла, графита или проводящей резины. Этот внешний электрод размещается в той же коррозионной среде, что и защищаемый объект, в случае подземных промысловых трубопроводов, в почве. Таким образом, образуется замкнутая электрическая цепь: дополнительный внешний электрод – почвенный электролит – трубопровод – катодный кабель – источник постоянного тока – анодный кабель. В составе данной электрической цепи трубопровод является катодом, а дополнительный внешний электрод, присоединенный к положительному полюсу источника постоянного тока, становится анодом. Данный электрод называется анодным заземлением. Отрицательно заряженный полюс источника тока, присоединенный к трубопроводу, при наличии внешнего анодного заземления катодно поляризует трубопровод, при этом потенциал анодных и катодных участков практически выравнивается.
Таким образом, система катодной защиты состоит из защищаемого сооружения, источника постоянного тока (станции катодной защиты), анодного заземления, соединительных анодной и катодной линий, окружающей их электропроводной среды (почвы), а также элементов системы мониторинга – контрольно-измерительных пунктов.
Дренажная защита от коррозии
Дренажная защита трубопроводов от коррозии блуждающими токами осуществляется путем направленного отвода этих токов к источнику или в землю. Установка дренажной защиты может быть нескольких видов: земляной, прямой, поляризованный и усиленный дренажи.

Рис. 3. Станция дренажной защиты
Земляной дренаж осуществляется заземлением трубопроводов дополнительными электродами в местах их анодных зон, прямой дренаж – созданием электрической перемычки между трубопроводом и отрицательным полюсом источника блуждающих токов, например рельсовой сетью электрифицированной железной дороги. Поляризованный дренаж в отличие от прямого обладает только односторонней проводимостью, поэтому при появлении положительного потенциала на рельсах дренаж автоматически отключается. В усиленном дренаже дополнительно в цепь включается преобразователь тока, позволяющий увеличивать дренажный ток.
Все стальные подземные газопроводы защищают от химической и электрической коррозий. Величина коррозии зависит от степени коррозионности грунтов.
Различают пассивную и активную защиту газопроводов от коррозии. Пассивная защита осуществляется покрытием стального газопровода противокоррозионной изоляцией, в качестве которой применяют битумное, битумно-резиновое и пластиковое покрытия, которые наносятся на трубы заводом-изготовителем.
Пассивная защита подземных газопроводов изолирующими покрытиями дополняется активной. Эти виды противокоррозионной защиты предотвращают действие почвенной коррозии и коррозии блуждающими электрическими токами, наводимыми на стальной газопровод электрифицированным транспортом.
Активная защита сводится в основном к электрической, задача которой – отвод блуждающих электрических токов с защищаемого газопровода и организованный возврат их к электроустановкам и сетям постоянного тока, являющимся источниками блуждающих токов; подавление протекающих по газопроводу токов в местах их выхода в землю (анодные зоны) токами от внешнего источника; предотвращение распространения электрических токов по системе газопровода путем секционирования последнего электроизолирующими устройствами (изолирующими фланцами).
Отвод блуждающих токов можно осуществить устройством дополнительных заземлений; простой или прямой дренажной защитой, т.е. электрическим соединением защищаемого газопровода с рельефом электрифицированного транспорта с целью возврата токов к их источнику; поляризованной дренажной защитой, т.е. дренажом с односторонней проводимостью, исключающей обратное течение тока от рельсов к защищаемому объекту; усиленной дренажной защитой, т.е. такой поляризованной защитой, в цепь которой для повышения эффективности включен внешний источник внешний источник постоянного тока, что представляет собой объединение поляризованного дренажа с катодной защитой. При дополнительном заземлении (катодная защита, рисунок 1а) защищаемый газопровод присоединяется к отрицательному полюсу внешнего источника тока в качестве катода, а положительный полюс – к специальному заземлению – аноду. При этом создается замкнутая цепь, в которой ток проходит от анода через землю к защищаемому трубопроводу и к отрицательному полюсу внешнего источника.
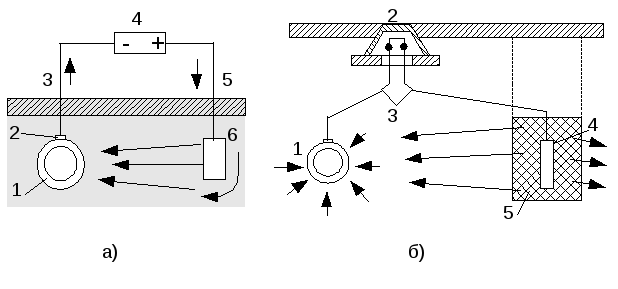
Рисунок 1 – Схемы усиленной дренажной защиты
а)катодная (1 –защищаемый газопровод; 2 – точка присоединения дренажного кабеля; 3,5 – дренажные кабели; 4 – внешний источник электрического тока; 6 – анодное заземление); б)протекторная (1 – защищаемый газопровод; 2 – контрольный вывод; 3 – изолированные кабели; 4 – протектор; 5 – заполнитель для протектора).
Наблюдается разрушение анодного заземления, а не газопровода (разрушение наблюдается в местах стока электрического заряда в землю). В качестве внешнего источника тока применяются специальные станции катодной защиты (СКЗ) разных конструкций.
Принципиальная схема протекторной защиты (рисунок 1б) предусматривает использование в электрической цепи протекторов из металла, обладающих по отношению к среде более высоким отрицательным электрохимическим потенциалов, чем материал газопровода. Электрический ток возникает в системе протекторной защиты также как в гальваническом элементе, причем электролитом служит грунт, содержащий влагу, а электродами – газопровод и протектор. Возникающий защитный ток подавляет токи электрохимической коррозии и обеспечивает создание защитного электрического потенциала на газопроводе.
Работа защитных установок подлежит систематическому контролю и измерениям службами горгаза в строго определенные сроки. Осмотры производят не реже двух раз в месяц, контрольные замеры токов и сопротивлений в дренажных установках и катодной защите – не реже одного раза в месяц, а измерение сопротивления анодному растеканию анодного заземления – не реже одного раза в 3 месяца.
Блог технической поддержки моих разработок
Больше 15 лет я разрабатываю станции катодной защиты. Требования к станциям четко формализованы. Есть определенные параметры, которые должны быть обеспечены. А знание теории защиты от коррозии совсем не обязательно. Гораздо важнее знание электроники, программирования, принципов конструирования электронной аппаратуры.
Создав этот сайт, я не сомневался, что когда-нибудь там появится раздел катодная защита. В нем я собираюсь писать о том, что я хорошо знаю, о станциях катодной защиты. Но как-то не поднимается рука писать о станциях, не рассказав, хотя бы коротко, о теории электрохимической защиты. Постараюсь рассказать о таком сложном понятии как можно проще, для не профессионалов.
История развития катодной защиты настолько занимательная глава, что я изложил ее в отдельной статье. Она не имеет практического значения. Просто интересно.
Для того чтобы защитится от коррозии, надо понять, что такое коррозия, природу ее происхождения.
Электрохимическая коррозия.
Коррозию можно определить как реакцию материала с окружающей средой, вызывающую в нем ощутимые изменения.
Изменения – понятие расплывчатое. Поэтому существует понятие коррозионного повреждения, основными признаками которого является нарушение функционирования объекта, например разрушение все той же металлической трубы. Не все реакции ведут к повреждению. Если труба станет коричневой или зеленой, но не будет протекать, это не будет считаться коррозионным повреждением.
Материалы и окружающая среда бывают разными. Бывают разными и реакции между ними. В основе коррозии могут лежать чисто химические реакции. Но вряд ли кого-либо заинтересует коррозия висмута в растворе дигидрофосфата натрия. Гораздо важнее знать о коррозии железной трубы, закопанной в землю.
Так вот, практический интерес имеет коррозия металлических материалов в водных средах, т.е. электрохимическая коррозия. В основе ее лежат реакции, имеющие электрохимическую природу.
В детстве я был любознательным мальчиком. Я проводил опыты по гальваническому осаждению меди на железные предметы, чем удивлял своих одноклассников. Но еще больше я поразил их, когда принес в школу лезвие от безопасной бритвы с вырезанной на нем сквозной надписью. Эффект я усилил сказав, что сделал это лазером. Конечно, я просто покрыл лезвие лаком, иголкой выцарапал надпись, опустил в жестяную банку с раствором соли, подключил электрический ток и немного подождал. Теперь я понимаю, что мои детские опыты были иллюстрацией того, как происходит электрохимическая коррозия и как от нее защититься. (Рассказ о моих детских опытах не художественный вымысел, а чистая правда.)
Итак, объекты процесса электрохимической коррозии:
- среда – раствор электролита (почва всегда влажная, поэтому это тоже раствор электролита);
- граница раздела среда-металл;
- металл.
Все перечисленные объекты способны проводить электрический ток, обладают хорошей электропроводностью. В растворе электролита содержатся анионы и катионы. Они создают электрический ток. Ток протекает через участок металл – раствор электролита. За счет этого тока на границе раздела происходит электрохимическая реакция, на которую могут влиять еще и внешние токи. Влиять они могут по-разному, как усиливать коррозию, так и замедлять ее.

За счет тока на границе образуется разность потенциалов. Ее невозможно измерить. Поэтому измеряют потенциал специального электрода сравнения. Он является своеобразным суммарным показателем электрохимической реакции.
Физическое объяснение электрохимической коррозии выглядит так. В металле присутствуют ионы железа (положительно заряженные) и электроны (с отрицательным зарядом). Оба компонента реагируют с раствором электролита.
- При положительном токе металл переходит в раствор, что связано с прохождения ионов и вызывает потерю массы металла (растворение металла).
- При отрицательном токе в раствор проходят электроны, и происходит это без потери массы металла.
В первом случае происходит анодная, а во втором случае – катодная электрохимические реакции. Анодная реакция (растворение металла) вызывает коррозию. Катодная реакция является процессом обратным коррозии и используется в гальванотехнике для нанесения гальванических покрытий.
Принцип действия катодной защиты.
Понятно, что для защиты объекта от коррозии необходимо вызвать катодную реакцию и не допустить анодную. Сделать это можно, если искусственно создать отрицательный потенциал на защищаемом объекте.
Для этого необходимо разместить в среде (почве) анодные электроды и подключить внешний источник тока: минус к объекту защиты, а плюс – к анодным электродам. Ток пойдет по цепи анодный электрод – почвенный электролит – объект защиты от коррозии.
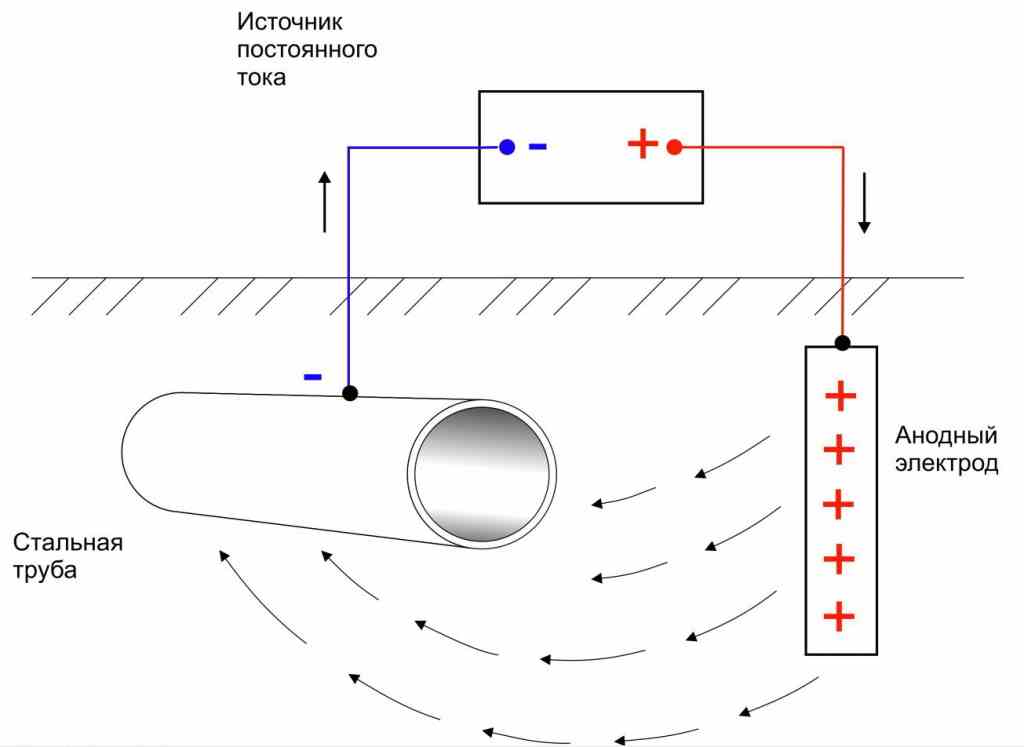
С точки зрения гальванических процессов металлический объект будет катодом, а дополнительный электрод – анодом.
Таким образом, коррозия объекта прекратится. Разрушаться будет только анодный электрод. Он называются анодным заземлением. Анодные электроды делают из инертного материала и периодически меняют.
Станция катодной защиты.
Ток для катодной защиты вырабатывает специальное устройство – станция катодной защиты.
По сути это источник вторичного электропитания, специализированный блок питания. Т.е. станция подключается к питающей сети (как правило
220 В) и вырабатывает электрический ток с заданными параметрами.
Вот пример схемы системы электрохимической защиты подземного газопровода с помощью станции катодной защиты ИСТ-1000.
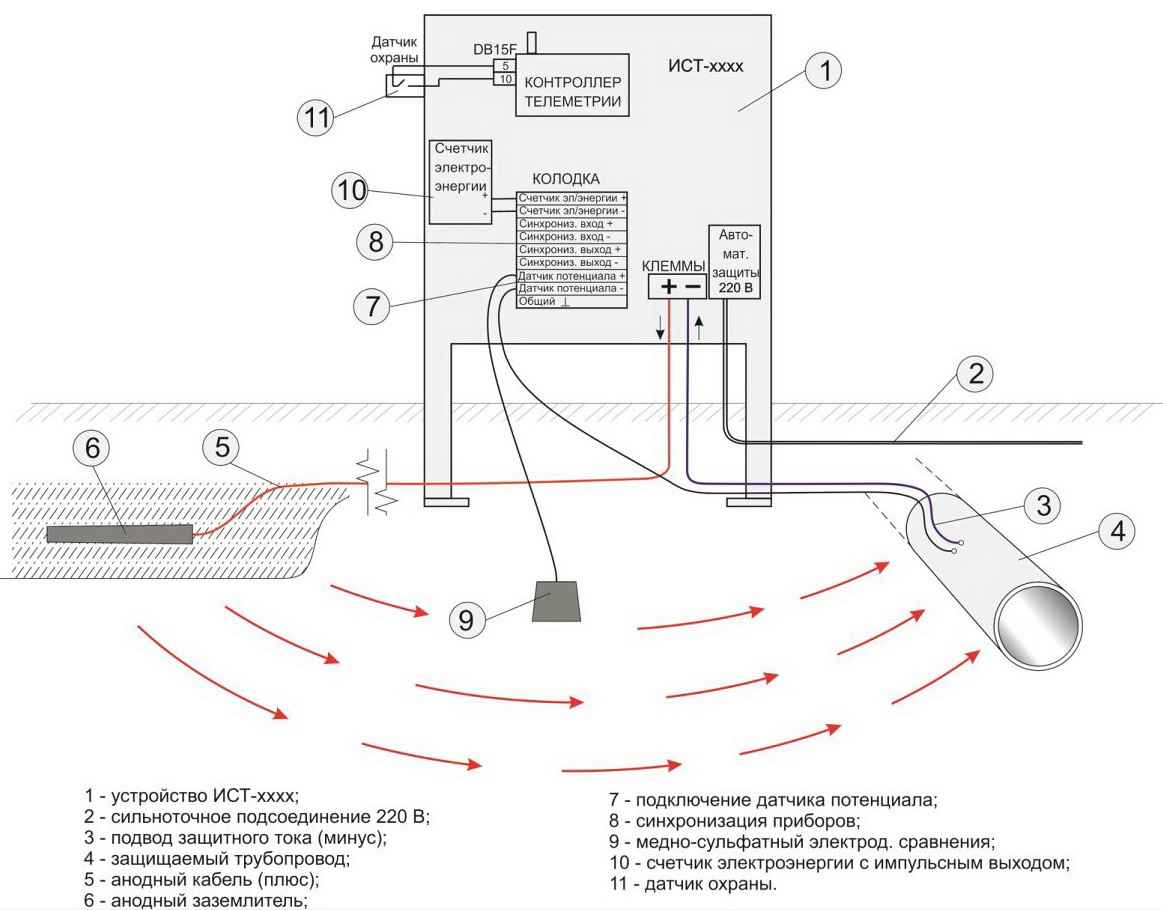
Станция катодной защиты установлена на поверхности земли, вблизи от газопровода. Т.к. станция эксплуатируется на открытом воздухе, то она должна иметь исполнение IP34 и выше. В этом примере используется современная станция, с контроллером GSM телеметрии и функцией стабилизации потенциала.
В принципе, станции катодной защиты бывают очень разными. Они могут быть трансформаторными или инверторными. Могут быть источниками тока, напряжения, иметь различные режимы стабилизации, различные функциональные возможности.
Станции прошлых лет это громадные трансформаторы с тиристорными регуляторами. Современные станции это инверторные преобразователи с микропроцессорным управлением и GSM телемеханикой.
Выходная мощность устройств катодной защиты, как правило, находится в диапазоне 1 – 3 кВт, но может доходить и до 10 кВт. Станциям катодной защиты и их параметрам посвящена отдельная статья.
Нагрузкой для устройства катодной защиты является электрическая цепь: анодное заземление – почва – изоляция металлического объекта. Поэтому требования к выходным энергетическим параметрам станций, прежде всего, определяют:
- состояние анодного заземления (сопротивление анод-почва);
- почва (сопротивление грунта);
- состояние изоляции объекта защиты от коррозии (сопротивление изоляции объекта).
Все параметры станции определяются при создании проекта катодной защиты:
- рассчитываются параметры трубопровода;
- определяется величина защитного потенциала;
- рассчитывается сила защитного тока;
- определяется длина защитной зоны;
- выбирается место установки станции;
- определяется тип, место расположения и параметры анодного заземления;
- окончательно рассчитываются параметры станции катодной защиты.
Применение.
Катодная защита от коррозии получила широкое распространение для электрохимической защиты:
- подземных газопроводов и нефтепроводов;
- трубопроводов теплосетей и водоснабжения;
- оболочек электрических кабелей;
- крупных металлических объектов, резервуаров;
- подземных сооружений;
- морских судов от коррозии в воде;
- стальной арматуры в железобетонных сваях, в фундаментах.
Применение катодной защиты обязательно для газопроводов низкого и среднего давления, магистральных газопроводов, нефтепроводов.
